Tudo sobre RDC 430 e RDC 653 da Anvisa [Guia prático + Prazos + Boas Práticas]
A Resolução de Diretoria Colegiada (RDC) 430 foi publicada em 2020 pela Anvisa, ficando conhecida por alguns profissionais como a RDC para distribuidora de medicamentos.
Nesse documento, o órgão regulador definiu uma série de Boas Práticas, processos e prazos necessários para a garantir a qualidade de medicamentos, seja no armazenamento ou nas rotas de transporte.
Acompanhe este guia preparado pela SyOS para conhecer em detalhes a RDC 430!
Guia prático: as principais dúvidas sobre a RDC 430/2020

Muitos profissionais têm dúvida se a RDC 430 foi revogada. A resposta é: não, ela apenas foi atualizada pela RDC 653, que está em vigor desde 16 de março de 2024.
Ambas as resoluções tratam sobre as ações necessárias para garantir a qualidade de medicamentos ao longo da cadeia de distribuição – especialmente os mais sensíveis à temperatura, como termolábeis. Confira!
A quem se aplica a RDC 430 e a RDC 653?
Também conhecida como a RDC para distribuidora de medicamentos, a resolução se aplica a todas as empresas que realizam a distribuição, a armazenagem ou o transporte de medicamentos. Desse modo, a norma determina que é função dessas empresas garantir a qualidade e a segurança dos medicamentos (Cap. II, Art. 4º).
Entretanto, essa função não se aplica às empresas que distribuem, armazenam ou transportam matérias-primas, gases medicinais ou rótulos para medicamentos (Art. 2º do Cap. I), já que essas atividades têm legislação específica.
O que a RDC 430 fala sobre equipamentos e sistemas informatizados?
A RDC 430 define que os equipamentos e sistemas informatizados precisam ser qualificados e validados antes de sua implementação e uso. Além disso, esses processos precisam ser refeitos quando mudanças significativas forem realizadas.
Outra definição da resolução da Anvisa é a realização de manutenção preventiva nos equipamentos que impactam na qualidade dos medicamentos. Desse modo, os riscos podem ser evitados antes que causem danos aos produtos ou à sustentabilidade das operações.
Monitoramento de temperatura e umidade de acordo com a RDC 430 para distribuidora de medicamentos
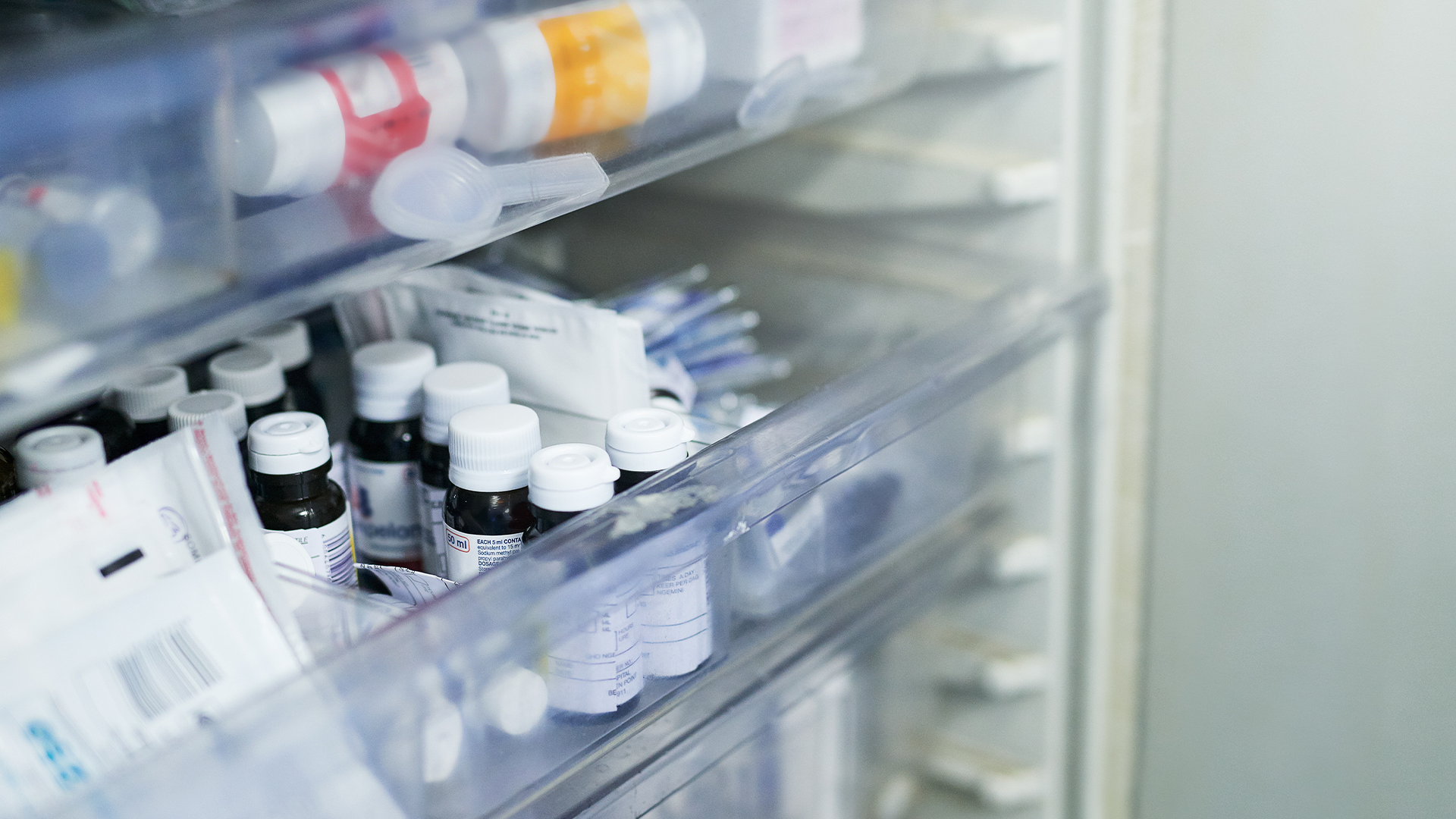
Segundo a RDC 430 de 2020, toda operação de monitoramento deve ser submetida a uma análise de riscos que determinará os equipamentos e sistemas informatizados a serem utilizados e que precisam ser qualificados e validados.
Em relação à armazenagem, o Art. 43 da Seção IV define:
- o uso de instrumentos adequados para controlar e monitorar temperatura e umidade de acordo com a qualificação térmica da área;
- a calibração de instrumentos antes do primeiro uso e a recalibração em intervalos definidos de acordo com o desempenho do instrumento e a sensibilidade da medida;
- o registro eletrônico dos dados de monitoramento com armazenagem de informações por dois anos após sua geração.
Já em relação à armazenagem em trânsito e ao transporte, o Art. 63 da Seção VII define que é responsabilidade da empresa que contrata o transportador qualificar o serviço de transporte.
Além disso, o Art. 63 da Seção VII também trata sobre as responsabilidades que a empresa contratada (transportadora ou distribuidora de medicamentos) tem durante a prestação do serviço, que incluem:
- monitorar as condições de transporte, incluindo temperatura e umidade, utilizando instrumentos calibrados;
- utilizar sistemas ativos ou passivos de controle de temperatura e umidade que sejam adequados para manter as condições necessárias de manutenção da carga de acordo com o registro sanitário ou outras especificações aplicáveis;
- fornecer os dados sobre as condições de conservação durante o transporte e também durante a armazenagem em trânsito.
O que a RDC 430 fala sobre os medicamentos termolábeis?
Na Seção IX da RDC 430, é definido que a exposição à temperatura ambiente deve ser minimizada durante o recebimento e a expedição dos medicamentos termolábeis.
Para isso, se necessário, áreas refrigeradas podem ser adotadas nos espaços de recebimento e expedição dos medicamentos. Outro procedimento necessário é o registro do tempo em que os medicamentos ficaram submetidos à temperatura ambiente.
Pensando na segurança dos medicamentos, também é necessário elaborar um plano de contingência caso haja falha no fornecimento de energia elétrica para o sistema de refrigeração. Por conta disso, os equipamentos precisam contar com uma fonte alternativa capaz de suprir energia.
Prazos da RDC 430 atualizada (RDC 653/2022): o que muda?

A RDC 430 para distribuidora de medicamentos ainda é a norma de referência para as atividades de armazenagem e transporte de medicamentos e vacinas sensíveis à temperatura e à umidade.
Porém, a RDC 653 de 2022 atualizou alguns prazos para a implementação de soluções de monitoramento. Confira as mudanças.
A primeira resolução (RDC 430) define implementação de uma série de medidas:
O Art. 89 define que as empresas envolvidas na cadeia de distribuição devem elaborar estudos de mapeamento de temperatura e umidade – como a análise de riscos, a qualificação térmica e o mapeamento de rotas. O objetivo desses estudos é indicar as medidas de controle ativo ou passivo necessárias no sistema de transporte.
Já o Art. 64 exige o cumprimento de dois incisos:
- Inciso II: monitorar as condições de transporte relacionadas às especificações de temperatura, acondicionamento, armazenagem e umidade do medicamento utilizando instrumentos calibrados;
- Inciso III: aplicar os sistemas passivos ou ativos de controle de temperatura e umidade que sejam necessários à manutenção das condições requeridas pelo registro sanitário ou outras especificações aplicáveis.
Com a publicação da RDC 653, os prazos para cumprir essas determinações foi prolongado. Confira o que diz a nova resolução:
- o prazo para a realização da análsie de riscos, do mapeamento de rotas e da qualificação térmica foi a data 16/3/2023 (já passou);
- o novo prazo para a implementação das medidas necessárias para o controle e monitoramento de temperatura de acordo com os estudos iniciais é data 16/3/2024 (já está em vigor — não foi revogada).
Sistema de Gestão da Qualidade (SGQ): o que a RDC 430 diz sobre

Um Sistema de Gestão da Qualidade tem como objetivo monitorar, corrigir e aperfeiçoar processos para garantir a qualidade de produtos e serviços, além de atender às normas e legislações e criar condições para a lucratividade das empresas envolvidas.
Em relação à armazenagem e distribuição de medicamentos, a RDC 430 define uma série de funções e responsabilidades do SGQ. Abaixo, você pode conferir algumas delas.
O que é necessário para implementar um Sistema de Gestão de Qualidade
Na Seção III da RDC 430, são definidas algumas ações necessárias para a implementação do SGQ. Confira as principais:
- é necessário mapear todos os processos que interferem na qualidade dos medicamentos;
- os processos mapeados devem ser geridos por Procedimentos Operacionais Padrão (POPs) com a geração de registros;
- ações que divergem do que é definido pelo Sistema de Gestão da Qualidade deverão ser consideradas não conformidades;
Entre outras ações necessárias.
Como é feita a documentação de um SGQ

Em relação aos registros do Sistema de Gestão da Qualidade, a RDC para distribuidora de medicamentos define que:
- os POPs devem ser atualizados para corresponder às práticas adotadas no dia a dia;
- os POPs devem ser compreensíveis aos envolvidos em cada processos, sem ambiguidades;
- os registros dos POPs devem ser mantidos por pelo menos 5 anos;
- os registros de dados devem ser recuperáveis e armazenados com medidas de segurança que impeçam a modificação não autorizada;
- a alteração de dados deve ser feita somente com justificativa e o dado original deve ser preservado.
As responsabilidades da área que controla o SGQ
A RDC 430 também descreve uma série de responsabilidades da área responsável pelo Sistema de Gestão da Qualidade (Seção III, Art. 18). Desse modo, a resolução define que essa área deve ter autonomia e recursos necessários para:
- garantir a implementação e a manutenção do SGQ;
- elaborar, revisar e aprovar os Procedimentos Operacionais Padrão (POPs);
- implementar e manter as autoinspeções;
- receber e investigar reclamações;
- garantir a integridade e a rastreabilidade dos medicamentos e dos dados relativos às transações comerciais;
- gerenciar ações corretivas para não conformidades.
Entre em conformidade com as RDC 430 e RDC 653 da Anvisa com a SyOS

Se você é um profissional da qualidade, operador logístico ou atua em um distribuidora de medicamentos, entrar em conformidade com a Anvisa é um dos seus objetivos nesse momento.
A SyOS tem uma solução de monitoramento de temperatura e umidade que une Internet das Coisas e Inteligência Artificial para controlar o acondicionamento de produtos farmacêuticos nos transportes, nos centros de distribuição e nas indústrias.
Confira alguns detalhes sobre nossa tecnologia:
- Sensores automáticos e conectados à internet;
- Dados sobre temperatura e umidade disponibilizados em tempo real para os gestores;
- Inteligência Artificial ativa 24 horas por dia, analisando os dados e emitindo alertas quando ocorrem variações que oferecem riscos aos produtos;
- Relatórios seguros e auditáveis para apresentar a clientes e fiscalizações.
Conheça nossa solução para o setor farmacêutico e descubra como o jeito SyOS de monitorar pode transformar a sua gestão da temperatura e da umidade.
Glossário: conheça os termos mais importantes usados pela RDC 430 da Anvisa

Se você é um profissional envolvido em qualquer atividade do setor farmacêutico, está familiarizado com termos e siglas específicos, como BPDA (Boas Práticas de Distribuição e Armazenagem) e POP (Procedimentos Operacionais Padronizados).
Mas sabemos que dúvidas podem surgir no dia a dia, especialmente para os profissionais que estão desbravando novas funções ou desafios. Por isso, preparamos um glossário com os principais termos e siglas abordados nas RDC 430 e RDC 653. Confira!
Cadeia do frio
O termo trata de uma rede interligada na qual cada elo representa um responsável pelo transporte ou a armazenagem de produtos com controle de temperatura. No caso da cadeia do frio de medicamentos e vacinas, os elos são os seguintes: indústrias, centros de distribuição e pontos de vendas; além disso, estes elos são interligados pelos operadores logísticos (OP).
Operador Logístico (OL)
São as empresas responsáveis pelo transporte de medicamentos que obtiveram as autorizações necessários para a prestação desse tipo de serviço.
Sistema de Gestão de Qualidade (SGQ)
Um Sistema de Gestão da Qualidade tem como objetivo implementar medidas padronizadas para garantir a qualidade e a eficácia de produtos e processos, além da sustentabilidade financeira e ambiental de uma organização.
Não conformidade e conformidade
As não conformidades são ocorrências operacionais que não correspondem aos padrões definidos para um processo. Esses padrões são definidos por normas e legislações e também pelo SQG de cada empresa. As conformidades, por outro lado, são operações realizadas de acordo com os padrões estabelecidos.
Medicamento(s) termolábil(eis)
São os medicamentos (ou vacinas) que têm uma faixa de temperatura bastante restrita para garantir sua eficácia. A faixa de temperatura para os termolábeis fica entre +2ºC e +8ºC.
Boas Práticas de Transporte (BPT)
As BPT são as ações que garantem a qualidade de medicamentos durante o transporte e também protegem o sistema de transporte de roubos, avarias ou adulterações.
Boas Práticas de Armazenagem (BPA)
São todas as ações que garantem a qualidade de um medicamento durante a armazenagem, assim como as ações que visam proteger o sistema de armazenagem de medicamentos falsos, reprovados, importados de maneira ilegal, roubados ou adulterados.
Boas Práticas de Distribuição e Armazenagem (BPDA)
Essa sigla define as ações que visam a qualidade dos medicamentos durante o transporte ou a armazenagem em trânsito, além da garantia de ferramentas de proteção desse sistema contra roubos, avarias e adulterações.
Procedimento Operacional Padrão/Padronizado (POP)
Conhecidos como “Pop da Anvisa”, é um procedimento escrito e autorizado que dá instruções sobre como as operações devem ser feitas. Alguns exemplos incluem os POPs para manutenção, limpeza, qualificação, inspeção, etc.
Qualificação térmica
A qualificação térmica é um processo de verificação documentada de que o equipamento ou a área de temperatura controlada são capazes de garantir a homogeneidade térmica do ambiente.
Sistema ativo de controle
Os sistemas ativos de controle são capazes de ajustar automaticamente a temperatura e a umidade de um ambiente, como os sistemas que usam fornecimento de energia elétrica para funcionar. Alguns exemplos incluem os contêineres refrigerados, as câmaras frias e os caminhões refrigerados.
Sistema passivo de controle
Os sistemas passivos não possuem a capacidade de ajuste automático da temperatura, a exemplo dos contêineres com isolamento térmico, feitos de poliestireno ou de material refrigerante. Por conta disso, sua capacidade de transporte refrigerado é menor. A adoção desses sistemas depende de estudos e previsões de temperatura e umidade que consideram as condições climáticas durante o transporte, o tipo de produto transportado, o tempo de rota, etc.
Sobre a SyOS
Somos uma startup que tem o objetivo de revolucionar a cadeia do frio no Brasil, através de tecnologias de IoT e Inteligência Artificial aplicadas no monitoramento de produtos que precisam de uma temperatura ideal para manter sua qualidade, como alimentos, vacinas e medicamentos.
Com isso, empresas que atuam com a gestão do frio têm acesso a dados, relatórios e alertas que ajudam a tomar decisões para otimizar suas operações, evitar a não conformidade e reduzir prejuízos.
Descubra mais sobre a SyOS ou entre em contato com o nosso time de especialistas para conhecer melhor nossa solução.

![[Grátis] RDC 430: Distribuidora de medicamentos e Transportadora Controle de temperatura de acordo com a Anvisa](https://no-cache.hubspot.com/cta/default/8356687/interactive-197771339293.png)