Controle de qualidade de medicamentos: funções, normas e monitoramento

Você sabe qual é a função do controle de qualidade de medicamentos? Este é um processo essencial para garantir que os fármacos sejam eficazes, não tenham impurezas nem tragam riscos à saúde quando chegarem ao consumidor em clínicas, hospitais ou farmácias.
Assim, para produzir medicamentos com as características desejáveis em larga escala, as indústrias farmacêuticas devem instituir um Sistema de Gestão da Qualidade (SGQ). Esse sistema determina a padronização de procedimentos e acompanha de perto sua execução em todas as etapas de fabricação, armazenagem e transporte.
Por isso, nesse texto, você vai conhecer melhor como funciona o controle de qualidade na indústria farmacêutica, sua importância para o sucesso operacional e variáveis que devem ser monitoradas, como a temperatura e a umidade nos ambientes que armazenam insumos e produtos farmacêuticos. Boa leitura!
O que é controle de qualidade de medicamentos?
De acordo com a RDC 658/22 da Agência Nacional de Vigilância Sanitária (ANVISA), o controle de qualidade de medicamentos é:
“Art. 13. O Controle de Qualidade é a parte das BPF (Boas Práticas de Fabricação) referente à coleta de amostras, às especificações e à execução de testes, bem como à organização, à documentação e aos procedimentos de liberação que asseguram que os testes relevantes e necessários sejam executados, e que os materiais não sejam liberados para uso, ou que produtos não sejam liberados para comercialização ou distribuição, até que a sua qualidade tenha sido considerada satisfatória.”
Dessa forma, o controle de qualidade analisa os aspectos físico-químicos e microbiológicos para assegurar a qualidade de produtos como:
- Medicamentos;
- Produtos biológicos;
- Insumos farmacêuticos.
Além disso, na prática, na indústria farmacêutica, o controle de qualidade de medicamentos tem uma ampla atuação, que inclui a análise de:
- Insumos;
- Materiais de embalagem;
- Produtos intermediários de produção;
- Produto acabando;
- Condições de transporte e armazenamento adequadas, etc.
Entre os parâmetros verificados estão: pureza, dose, e os perfis de desintegração, dissolução e microbiológico. Dessa forma, essas análises servem para identificar desvios, mapear mudanças ou até interromper a fabricação.
Isso porque a ANVISA regulamenta de maneira rigorosa e extensa a produção de medicamentos no Brasil. Assim, o órgão fiscaliza intensamente as indústrias farmacêuticas quanto às boas práticas de fabricação e ao controle de qualidade.
Qual é a função do controle de qualidade?

Na indústria, o controle de qualidade integra o Sistema da Gestão da Qualidade Farmacêutica (SGQ). Assim, esse setor fica responsável por fazer análises de todos os processos produtivos.
Porém, essa responsabilidade exige que a área tenha autonomia em relação à produção. Apenas assim poderá se certificar de que os produtos realmente cumprem os requisitos mínimos de qualidade e, por isso, poderão seguir para as próximas etapas de produção.
Para cumprir esse objetivo, o controle de qualidade realiza atividades como:
- Definir especificações para procedimentos e produtos;
- Criar, legitimar e executar processos de controle;
- Realizar testes de qualidade;
- Controlar a referência e a retenção de amostras;
- Realizar investigações sobre reclamações relacionadas à qualidade dos produtos;
- Organizar a documentação para a liberação de produtos;
- Garantir que a etiquetagem dos produtos esteja correta, etc.
Assim, todas as tarefas de controle de qualidade de medicamentos devem ser realizadas com base em Procedimentos Operacionais Padronizados (POPs). Além disso, esses procedimentos devem ser preestabelecidos e devidamente registrados.
TIRE TODAS AS SUAS DÚVIDAS: Entenda o que é POP!
Qual é a importância do controle de qualidade na indústria farmacêutica?
O controle de qualidade de medicamentos é fundamental para a indústria farmacêutica. Isso porque sua principal função é atuar na prevenção de erros que possam comprometer a segurança dos pacientes.
Além disso, o setor é responsável por detectar com rapidez e eficácia as possíveis falhas no processo de produção de produtos de saúde. Dessa maneira, ao identificar deficiências de maneira precoce, a área pode implementar estratégias eficazes para resolver problemas imediatamente.
Por isso, os profissionais da área devem ter profundo conhecimento das normas reguladoras e se dedicar a cumpri-las.
Qual o papel da Anvisa no controle de medicamentos?
A ANVISA é um órgão regulador do Estado Brasileiro que, de acordo com sua própria definição:
“Tem por finalidade institucional promover a proteção da saúde da população, por intermédio do controle sanitário da produção e consumo de produtos e serviços submetidos à vigilância sanitária, inclusive dos ambientes, dos processos, dos insumos e das tecnologias a eles relacionados, bem como o controle de portos, aeroportos, fronteiras e recintos alfandegados.”
Sua atuação é bastante ampla, e o órgão exerce um papel central no controle sanitário de medicamentos, cosméticos e alimentos. Além disso, atua na promoção da saúde pública e na vigilância de fronteiras, portos e aeroportos brasileiros.
Assim, o papel da ANVISA no controle de medicamentos inclui:
- Definição de regulamentações abrangentes para a produção, a distribuição, a comercialização e o uso de medicamentos;
- Regulamentação detalhada de bulas e rótulos de medicamentos;
- Análise de documentos técnicos e informações de segurança para autorizar ou restringir a comercialização de vacinas;
- Desenvolvimento e atualização da Farmacopeia Brasileira, documento que reúne todas as normas e orientações para medicamentos e insumos farmacêuticos no Brasil;
- Investigação de denúncias sobre irregularidades em estabelecimentos relacionados à saúde da população.
Como é feito o controle de qualidade de medicamentos?
O controle de qualidade de medicamentos tem como base técnicas e estratégias específicas. Porém, normalmente, cumpre o seguinte processo:
- Realização de auditorias – De maneira frequente para garantir que a empresa esteja em compliance com as Boas Práticas de Fabricação (BPF) e outras normas;
- Criação de documentos e registros – Com o intuito de assegurar a rastreabilidade de todas as etapas dos processos;
- Realização de testes – Físico-químicos e microbiológicos nos produtos para garantir pureza, qualidade e conformidade com os regulamentos;
- Monitoramento de parâmetros críticos de fabricação – Como pressão, tempo de reação, temperatura e outros;
- Determinação de limites de impurezas – Para garantir a integridade dos medicamentos.
TIRE SUAS DÚVIDAS: Saiba tudo sobre o controle de temperatura na gestão da qualidade!
Boas Práticas e requisitos mínimos para o controle de qualidade
O controle de qualidade de medicamentos é essencial para garantir a eficácia dos fármacos. Porém, para garantir o cumprimento de suas funções, o SGC deve seguir Boas Práticas e requisitos mínimos. Assim, os principais são:
- Contar com equipe qualificada e realizar treinamentos para garantir o bom desempenho de todas as atividades;
- Possuir instalações, áreas, serviços e equipamentos adequados;
- Registrar procedimentos e desvios;
- Usar os materiais, rótulos e recipientes corretos;
- Possuir instruções procedimentos em conformidade com o Sistema da Qualidade Farmacêutica;
- Possuir armazenagem e transporte adequados.
Além disso, monitorar as condições ambientais na fabricação e armazenagem e transporte de medicamentos é fundamental para as Boas Práticas de Fabricação (BPF). Continue a leitura e entenda mais sobre esse tópico.
Principais normas e legislações para o controle de qualidade de medicamentos

A ANVISA é o principal órgão regulador do controle de qualidade de medicamentos no Brasil. Assim, a Resolução de Diretoria Colegiada (RDC) 658 do órgão é a norma mais importante para o controle de qualidade farmacêutico atualmente.
Também conhecida como a RDC de Boas Práticas de Fabricação (RDC BPF), essa resolução foi publicada em 2022 e atualiza normas anteriores, como a RDC 301. Além disso, a norma descreve de forma minuciosa o que é necessário para garantir a qualidade na fabricação de medicamentos por meio de um SGQ que implementa melhorias contínuas nos processos.
Assim como ela, também se destacam as RDCs 430 e 653. Saiba mais sobre essas regulamentações:
RDC 658 e o monitoramento contínuo na fabricação
Um dos temas mais importantes da RDC 658 é a necessidade de documentação de todas as atividades do Sistema de Gestão Qualidade farmacêutico. Além disso, o acompanhamento constante de sua efetividade com o uso de sistemas eficazes de monitoramento e controle de processos também tem destaque.
Com esse monitoramento, é possível chegar em critérios que ajudarão em aspectos como:
- Liberação de lotes de medicamentos;
- Investigação de desvios no padrão de qualidade;
- Realização de ações preventivas (CAPAs) com o objetivo de evitar desvios.
Além disso, a RDC 658 determina que o monitoramento deve ser aplicado nos ambientes de fabricação e de armazenamento. Porém, também deve ser estendida aos prestadores de serviços terceirizados relacionados às BPF.
Ou seja, as indústrias podem exigir a rastreabilidade de dados de monitoramento inclusive de parceiros que cuidam do armazenamento e distribuição de seus produtos.
Para entender melhor isso, conheça com mais detalhes as RDCs que tratam sobre as atividades de transporte e armazenagem.
RDC 430 e RDC 653: monitoramento no transporte e na armazenagem
A RDC 430/2020 e a RDC 653/2022 também são muito importantes para o controle de qualidade farmacêutico. Isso porque complementam a RDC específica para a fabricação, trazendo definições importantes para o transporte e a armazenagem de medicamentos.
Veja alguns detalhes dessas regulamentações:
- Boas Práticas de transporte e armazenagem;
- Exigência de controle e monitoramento de temperatura e umidade;
- Especificações para garantir a qualidade de produtos termolábeis;
- Adoção de sistemas passivos ou ativos de controle de temperatura e umidade;
- Prazos para realizar a qualificação térmica de rotas;
- Prazos para a adoção de soluções de monitoramento de temperatura e umidade;
- Entre outras definições importantes para garantir a qualidade de produtos farmacêuticos sensíveis à temperatura e umidade no transporte e na armazenagem.
DOWNLOAD GRATUITO: Baixe agora nosso ebook e saiba mais sobre a RDC 430!
Relação entre controle de qualidade e condições ambientais
Se as condições ambientais afetam os produtos, da mesma forma, é necessário controlá-las e avaliá-las continuamente.
Temperatura e umidade são dois exemplos de variáveis que impactam diretamente na qualidade. Além disso, a essa lista, podemos somar outras como a ventilação dos ambientes, a iluminação, a presença de vibração, interferências elétricas e até mesmo a limpeza (em relação à presença de microrganismos e impurezas no ambiente).
Ao ter dados sobre essas condições, os profissionais do controle de qualidade conseguem entender e agir sobre qualquer evento que afete a qualidade dos produtos, evitando não conformidades.
Para entender com mais detalhes as regras para o monitoramento dos ambientes, conheça algumas resoluções da Anvisa que devem ser seguidas pelo controle de qualidade farmacêutico.
Processos do controle de qualidade de medicamentos
A Organização Mundial da Saúde (OMS) possui um guia de Boas Práticas para laboratórios de controle de qualidade de produtos farmacêuticos. Desse modo, suas diretrizes têm como objetivo garantir a segurança e a qualidade dos medicamentos.
As instruções englobam toda a cadeia de produção: desde a matéria-prima dos medicamentos até o produto final. Além disso, são essenciais para garantir que os medicamentos sejam seguros e eficazes.
Os processos de controle de qualidade de medicamentos seguem quatro classificações. Saiba mais sobre cada uma delas:
1. Gestão e infraestrutura
Traz especificações sobre a infraestrutura e a equipe de gestão dos laboratórios de fabricação de medicamentos. A lista inclui itens como:
- Pessoal técnico e gerencial que tenha recursos e autoridade para realmente executar suas tarefas;
- Política de confidencialidade clara e com procedimentos adequados relacionados a dados e autorizações.
2. Materiais, instrumentos, equipamentos e outros
Ressalta a necessidade de identificar ou codificar instrumentos e equipamentos que exijam calibração. Exemplos de equipamentos assim são dispensers automáticos e vidrarias volumétricas.
A identificação é fundamental para refletir o estado da calibração, e deve conter o registro da data da última recalibração. Também é necessário realizar qualificações que incluem aspectos de:
- Projeto;
- Instalação;
- Operação;
- Desempenho dos equipamentos.
Por fim, também traz a necessidade de desenvolver procedimentos individuais para cada tipo de equipamento de medição. Para isso, é necessário considerar as características do equipamento, frequência de uso e diretrizes do fabricante.
3. Procedimentos de trabalho
Estabelece um formulário padrão que deve acompanhar cada amostra que ficar retida no laboratório. O formulário deve conter os seguintes dados:
- Nome da instituição ou do fiscal que remeteu a amostra;
- Origem do material;
- Descrição completa do fármaco, que inclui: composição, denominação comum internacional (DCI), se estiver disponível, e marca;
- Fórmula farmacêutica, conteúdo ou concentração, número de lote, se estiver disponível, fabricante e número de autorização de comercialização;
- Volume da amostra;
- Motivo da solicitação de análise;
- Data de coleta da amostra;
- Data de validade, para produtos farmacêuticos, ou de reanálise, para excipientes farmacêuticos e princípios ativos;
- Especificações que serão usadas nas análises;
- Métodos de análise que serão utilizados;
- Comentários adicionais;
- Condições de armazenamento.
4. Biossegurança
Determina que todos os membros da equipe possam acessar instruções de biossegurança que reflitam os riscos identificados. Para isso, podem utilizar cartazes, recursos audiovisuais, outros materiais impressos e seminários.
Além disso, os laboratórios devem fornecer equipamentos de proteção individual (EPIs) que incluam proteções para os olhos, mãos e face. Outro ponto é que devem instalar chuveiros de emergência, por precaução.
Por fim, a determinação exige que as equipes sejam treinadas para manipular vidrarias, solventes e reagentes corrosivos de maneira segura. Assim, o principal foco está no uso de embalagens de segurança e bandejas para evitar derramamentos de produtos.
SAIBA MAIS: Descubra por que a biossegurança é tão importante na saúde e no setor farmacêutico!
Desafios e oportunidades do controle de qualidade de medicamentos
Confira os principais desafios e oportunidades relacionados ao controle de qualidade de medicamentos:
Estrutura
O setor farmacêutico é obrigado a seguir um rigoroso padrão de qualidade. Nesse sentido, o principal desafio está em manter os ambientes extremamente limpos, e no caso da produção de fármacos injetáveis, estéreis.
Inovação
Para garantir o alto controle de qualidade, é necessário contar com instrumentos com tecnologia avançada para a produção. Nesse contexto entram equipamentos que permitem o acompanhamento da produção em tempo real.
Além disso, os sensores de monitoramento de itens como a temperatura ambiente são essenciais. Outro exemplo são laboratórios que já utilizam uniformes estéreis com tecnologia de última geração.
Conheça o sensor de temperatura e umidade IoT da SyOS e descubra como inovar no controle de qualidade de medicamentos!
Segurança
Para priorizar a segurança do produto, é fundamental certificar a pureza e a concentração exata de cada matéria-prima. Para que isso ocorra, os setores podem contar com equipamentos de alta tecnologia para detectar, identificar e qualificar a presença de impurezas tanto em matérias-primas quanto em produtos acabados.
Matéria-prima
Outro desafio é a qualificação dos fornecedores de matérias-primas. Para se destacar e garantir qualidade, os laboratórios podem realizar testes de controle de qualidade físico-químico e microbiológico para aprovar as matérias-primas de seus fornecedores.
Equipe multidisciplinar
Contar com uma equipe multidisciplinar é uma oportunidade de aumentar a eficácia da qualidade dos medicamentos. Assim, as equipes formadas por médicos, engenheiros e farmacêuticos, por exemplo, podem melhorar os processos e garantir a qualidade da produção.
Treinamento constante
Por fim, é essencial treinar e monitorar constantemente a produção dos medicamentos. Os profissionais devem tomar muito cuidado e atuar intencionalmente para reduzir a geração e o desprendimento de partículas.
Isso é fundamental, pois o principal fator de contaminação em ambientes de produtos estéreis é o fator humano.
O futuro do controle de qualidade de medicamentos
Diante de tudo isso, é evidente que, cada vez mais, a indústria farmacêutica pode se beneficiar da transformação digital e de tecnologias de automação. Isso porque essas ferramentas criam oportunidades de inovação para ampliar a capacidade do controle de qualidade.
Tecnologias de análise de dados, robótica e conectividade prometem revolucionar as práticas laboratoriais nos próximos anos. Dessa forma, soluções tecnológicas trazem diversos ganhos para a indústria farmacêutica, como:
- Redução de erros;
- Mitigação das variabilidades que existem em processos manuais;
- Prevenção de problemas de conformidade;
- Economia de custos.
Além disso, adotar sistemas tecnológicos em etapas importantes da produção de medicamentos traz vantagens tanto para o fabricante como para o usuário final. Exemplo disso é o monitoramento constante da temperatura e da umidade.
Dessa maneira, o futuro do controle de qualidade de medicamentos está diretamente relacionado aos investimentos em tecnologia. Em especial, quando se trata de ferramentas de fácil acesso e que trazem um significativo avanço aos processos.
SyOS: solução eficiente para o controle de temperatura de medicamentos
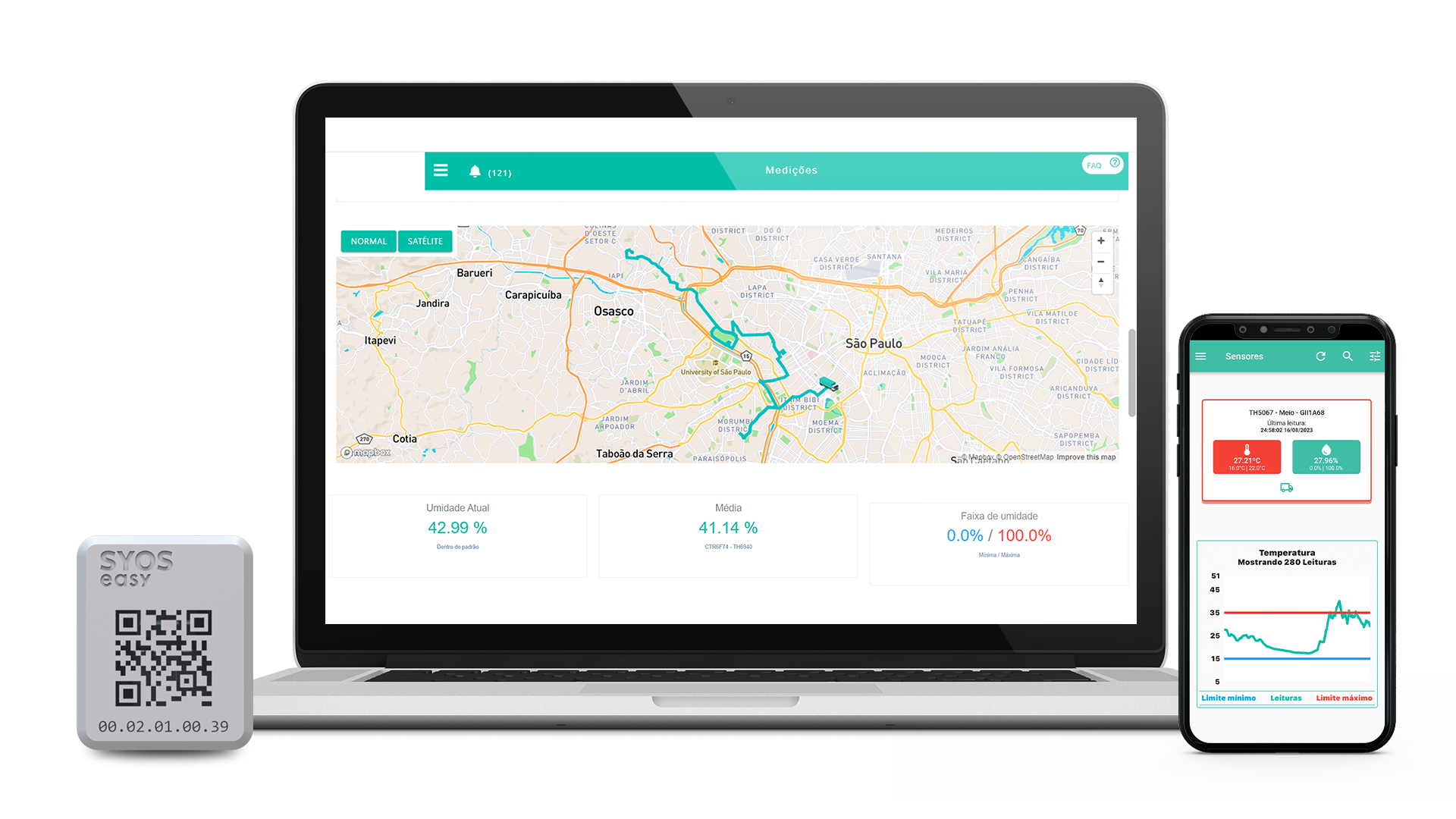
Ciente da importância do controle de qualidade de medicamentos, a SyOS desenvolveu uma tecnologia de monitoramento de temperatura e umidade 24×7. Para isso, utiliza Internet das Coisas (IoT) para disponibilizar dados em tempo real e sem processos manuais.
Com essa solução, o SGQ elimina processos manuais e evita erros na coleta de dados usando sensores automáticos e inteligentes.
Além disso, o acesso a dados em tempo real aumenta a capacidade preditiva do SGQ. Assim, os profissionais podem visualizar desvios em potencial com antecedência, acionar ações preventivas e evitar desvios e não conformidades.
Conheça a solução da SyOS para o setor farmacêutico e transforme o seu controle de qualidade.
Quer saber mais sobre o controle de qualidade de medicamentos? Continue acompanhando o blog da SyOS!
Glossário: conheça os principais termos sobre o controle de qualidade farmacêutico

Para te ajudar a entender melhor alguns termos importantes para o controle de qualidade, a SyOS criou um glossário baseado na RDC 658/2022 da Anvisa. Confira o glossário na íntegra! Abaixo, você tira suas dúvidas sobre os principais itens do glossário:
Sistema de Ação Corretiva e Ação Preventiva (CAPAs)
Processos que usam ferramentas de gestão da qualidade ou de gerenciamento de riscos para identificar, avaliar e investigar eventos com o objetivo de evitar reincidências.
Validação
Ação que comprova que procedimentos, processos, equipamentos, materiais, atividades ou sistemas realmente geram os resultados esperados.
Conformidade e não conformidade
Procedimentos executados ou não conforme os padrões estabelecidos pelo Sistema da Gestão da Qualidade (SGQ).
LEIA A ÍNTEGRA DESSE CONTEÚDO: Confira nosso glossário aqui!
Sobre a SyOS
Somos uma startup que tem o objetivo de revolucionar a cadeia do frio no Brasil, através de tecnologias de IoT e Inteligência Artificial aplicadas no monitoramento de produtos que precisam de uma temperatura ideal para manter sua qualidade, como alimentos, vacinas e medicamentos.
Com isso, empresas que atuam com a gestão do frio têm acesso a dados, relatórios e alertas que ajudam a tomar decisões para otimizar suas operações, evitar a não conformidade e reduzir prejuízos.
Descubra mais sobre a SyOS ou entre em contato com o nosso time de especialistas para conhecer melhor nossa solução.
![[Grátis] POP farmácia PDF + Planilha de temperatura Otimize o controle de temperatura em geladeira de farmácias com esse material gratuito e editável](https://no-cache.hubspot.com/cta/default/8356687/interactive-197773046802.png)

![[Grátis] E-Book Controle de qualidade: você sabe melhorar processos? Nesse material gratuito, você tem acesso a boas práticas e informações para saber como melhorar os processos da área da qualidade no dia a dia](https://no-cache.hubspot.com/cta/default/8356687/interactive-197782360227.png)